荣昌生物维迪西妥单抗一项联合用药 Ⅱ 期临床研究获批,该药品临床试验表现如何?
2022年最有潜力的创新药国产靶点有哪些?
近两年来,各行各业都受到COVID-19的冲击,国内创新药公司如雨后春笋一般涌现,靶点的研究与开发逐渐成为全国乃至全球的药物研发竞争点之一,目前靶点的研究与开发越来越同质化,赛道竞争越加激烈,2022年药企在选择适合自己研发的靶点时,应瞄准国内最有潜力的“中国新”靶点。
回顾2016-2021年,短短6年,我国便已上市66款国产1类新药上市(化药和生物类似药),国内Ⅰ类新药受理数量逐年提高;其中,2020 年申请受理数量相较以往增幅最大(增长 83%),反映出 CDE 效率和市场活跃度的大幅提升;2021 年Ⅰ类新药申请受理数量保持增长,申请受理数量同比 2020 年增长 68%,合计达到 1379 件。
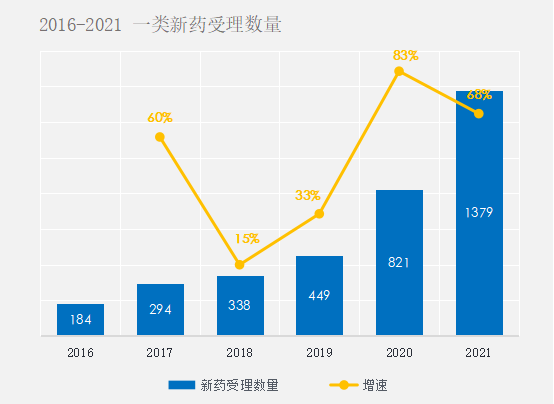
药融云中国1类新药靶点白皮书
在2016-2021 期间合计受理新药(1649个)涉及的靶点有 520 个;其中新药靶点同质化严重,前 6% (30) 的靶点涉及 41%(681) 的新药,在这些热门靶点,过半的靶点都与抗肿瘤靶点有关,其中神经系统用药、免疫调节、感染类、消化系统用药这四大领域相关靶点占比较大。
从中国1类新药靶点白皮书中得知,2016-2021期间国内新药涉及靶点top30,仅6%的靶点受理新药数量为41%。其中热门靶点扎堆,赛道拥挤,同质化问题越来越严重,在2022年甚至未来急需发现“中国新”靶点。
赛道为先,靶点为王,需要拒绝同质化,找寻出研究价值更大,市场前景更优的靶点信息。
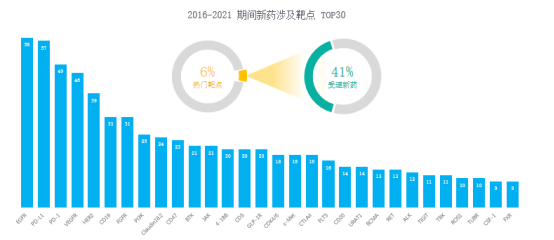
药融云中国1类新药靶点白皮书
拒绝同质化扎堆 寻找“中国新”靶点
“中国新”靶点的意义:用全球药物研发 IND 以上的靶点除去中国药物 IND 以上所涉及的靶点,得到的就是“中国新”靶点;
靶点在全球范围内已经有药物处于 IND 以上阶段,即在成药性上获得了一定的验证;排除国内在IND以上药物涉及靶点,即国内还没有该靶点的药物处于 IND 以上阶段;排序后,得到“中国新”靶点中的热门,研究价值更大;市场前景更优。
现代药物研发,源于靶点的选择,快速寻找到“中国新”靶点才是未来药物研发企业的发展趋势,,目前针对这些中国一类靶点白皮书总结了一些“中国新”靶点数据如图,药企可结合自身条件(方向、实力)等选择最优的靶点。
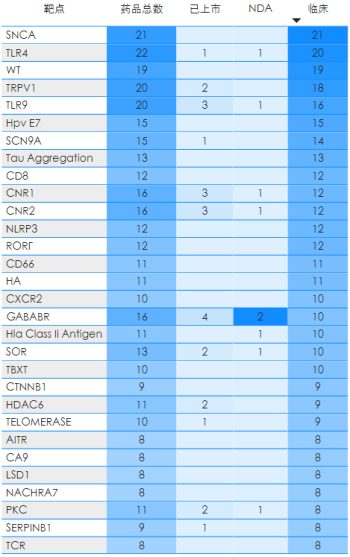
药融云中国1类新药靶点白皮书
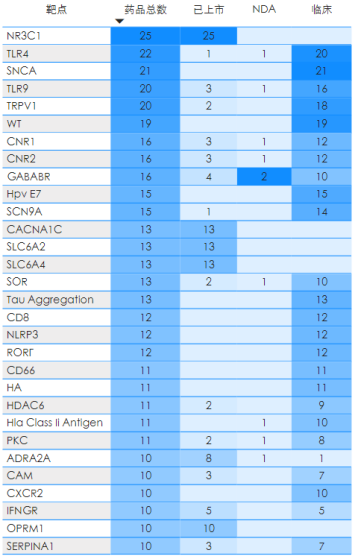
药融云中国1类新药靶点白皮书
通过以上数据可以分析选择2022年国内最具有潜力“中国新”靶点,再利用当前政策鼓励创新,拒绝盲目跟风热门靶点,提倡差异化创新等,结合公司自身的战略适配性,选择有价值,市场前景更优的靶点信息进行深一步的研究。
赛道为先,靶点为王,拒绝同质化、跟随政策创新和2022年国内最具有潜力“中国新”靶点,解决“新药研发进度赶不上市场发展速度”的问题,面对大量未被满足的临床需求,率先上市的一批药品大概率有更高的市场份额。
通过中国“新靶点”结合药融云数据库准确、高效、快速的掌握新靶点的信息、全球药物研发不同阶段占比、申报、专利、处方工艺、原料药用量、市场信息等等,查询针对这些靶点开发的主要领域、市场、专利、原料药等信息,再通过流行病学数据以及与公司自身的战略适配性,来选择靶点进行深一步研究。
HER2膀胱癌用维迪西妥单抗有效吗?
大量的临床数据已经证实,HER2有表达的膀胱癌用维迪西妥单抗会取得不错的效果。 早在2017年11月的时候,我国药企荣昌生物就已经启动了治疗尿路上皮癌的II期临床试验;而在2020年4月,维迪西妥单抗又获得FDA HER2阳性局部晚期或转移性尿路上皮癌Ⅱ期临床许可。5个月后,维迪西妥单抗正是被美国FDA授予治疗HER2阳性局部晚期或转移性尿路上皮癌的突破性疗法认定和快速审批通道资格。2021年6月,我国药企自主研发的新一代ADC药物获得中国药监局上市批准。正是基于在HER2膀胱癌治疗上的卓越疗效,维迪西妥单抗才能够成为首个同时获得中国国家药品监督管理局药品审评中心(CDE)和美国食品药品监督管维迪西妥单抗会不会成为新一代膀胱癌靶向药?
事实上维迪西妥单抗已经凭借优异的临床研究数据表现,成为新一代的膀胱癌靶向药中的佼佼者,而且效果显著。 自从正式获批上市以来,维迪西妥单抗的好消息就不断传出。根据已有的临床数据显示,维迪西妥单抗和HER2亲和力强,毒素抑瘤作用好,其“旁观者效应”可以杀伤HER2低表达肿瘤细胞,且药物抗体比例(DAR)为4,安全性更好。在Ⅱ期RC48-C005研究中,43例既往接受过至少一线系统化疗的HER2阳性(免疫组化[IHC]2+或3+)晚期尿路上皮癌患者接受维迪西妥单抗治疗,客观反应率(ORR)达到51.2%,疾病控制率(DCR)90.7%,中位无进展生存期(PFS)6.9个月,中位总生存期(OS)13.胃癌ADC靶向药维迪西妥单抗的效果确实不错吗?
在围绕着维迪西妥单抗开展的多个关键性研究中,这个胃癌ADC靶向药的数据都比较可观,从当前临床上来看,维迪西妥单抗在HER2晚期胃癌的治疗上有着出色的发挥。𰤴 所以现在完全可以说,维迪西妥单抗就是一款非常值得期待的好药。 值得关注的是,维迪西妥单抗这款胃癌ADC靶向药是一款完全由我国公司自主研发的新一代ADC药物。基于十多年的深厚布局,荣昌生物成功研发出了维迪西妥单抗,并且采用了新一代的药物成分,因此在效果上也有着更进一步的表现。据我了解,维迪西妥单抗采用了人表皮生长因子受体-2作为制导系统,通过连接子将单甲基奥瑞他汀E连接在一起,当精准进入癌细胞之后,维迪西妥单抗就会释放出非常强制药工程行业现状及前景
——预见2023:《2023年中国抗体偶联药物(ADC)行业全景图谱》(附市场现状、竞争格局和发展趋势等)
行业主要上市公司:荣昌生物(688331),恒瑞医药(600276)、科伦药业(002422)等
本文核心数据:抗体偶联药物行业市场规模、抗体偶联药物上市情况
行业概况
1、定义
抗体偶联药物(Antibody-Drug
Conjugates,ADCs)是一类由单克隆抗体和具有强效细胞毒性的小分子药物通过生物活性连接子偶联而成的新型生物药物。其药物作用机理为通过单克隆抗体特异导向靶标癌细胞,再由偶联的小分子药物杀死癌细胞。因此,ADC兼具了单克隆抗体药物高度特异性和靶向性的特点,以及小分子药物清除癌细胞的高效性,能协同发挥抗体药物和化学药物各自的优点,能够降低对生物系统的伤害。
ADC 药物由抗体、连接子、效应分子(小分子细胞毒药物)三个部分组成:
2、产业链剖析:中游环节涵盖创新药研发上市全流程
抗体偶联药物产业链全景图上游主要为抗体药物原材料,包括化学试剂、药物载体等,以及设备供应商;中游主要流程包括创新药研发、临床研究、临床试验、生产申报、规模化生产能等,参与者有高校、科研院所、制药企业、医药外包服务企业等;下游主要通过医疗机构治疗患者。
抗体偶联药物产业链全景图上游原材料供应商主要有健顺生物、金斯利等,设备供应商主要有华大智造、金仪盛世等;中游参与者主要有科伦博泰、荣昌生物、齐鲁制药等;下游医疗机构有中国疾病预防控制中心、北京大学肿瘤医院等。
行业发展历程:从理论走向实践
ADC药物的概念超前提出于1900年,但由于技术限制只能停留于理论层面。1990-2000 年间,单抗药物获得广泛的临床应用,为ADC
药物的研究提供契机。
行业政策背景:广泛受到政策支持
抗体偶联药物属于生物医药范畴,近年来,我国生物医药相关政策不断出台,从规划、行业规范、准入门槛等各维度进行的政策支持以及引导。2021年3月,全国人大发布《“十四五”生物医药产业发展规划》,从顶层设计将生物医药再次放到国家战略性新兴产业地位。
行业发展现状
1、抗体偶联药物技术发展
ADC技术的发展历程可大致分为4个阶段,第四代的ADC代表性品种有三个,分别为Enhertu、Trodelvy和SKB264,其中Enhertu重新定义了乳腺癌的治疗方式,正在冲击一线疗法;Trodelvy是首个针对三阴性乳腺癌的ADC药物,并取得了210亿美元的交易额;SKB264临床效果确切,相关技术平台实现了与MNC的巨额交易。这些ADC药物疗效显著,未来拥有巨大的想象空间。
2、抗体偶联药物市场占比情况
根据Frost&Sullivan分析,虽然抗体药物的市场主导是单抗药物,但ADC药物的成长性较大。2021年全球ADC药物市场份额约占抗体药物市场的3%,且预计到2030年将增长至14%;而中国的ADC药物市场份额上升空间更大,有望从2021年的1%上升至2030年的14%。
3、抗体偶联药物获批上市情况
截至2022年底,全球已有15款ADC药物获批上市,治疗疾病涉及淋巴瘤、白血病、乳腺癌、多发性骨髓瘤、乳腺癌、头颈癌、尿路上皮癌等。
截至2023年3月,中国市场获批的ADC药物有7个,分别是罗氏的恩美曲妥珠单抗、Seagen/武田的维布妥昔单抗、辉瑞的奥加伊妥珠单抗、荣昌生物的维迪西妥单抗、Immunomedics的戈沙妥珠单抗(该产品已被云顶新耀退回)、罗氏的维泊妥珠单抗、阿斯利康/第一三共的德曲妥珠单抗。
在全球15款获监管部门批准上市的ADC药物中,以HER2为靶点的数量排名第一,共计3款;以CD22为靶点的排名第二,有2款;另共有13款为传统小分子payloadlinker,其中,毒素方面,MMAE/MMAF类有6款,喜树碱类、卡奇霉素类、Maytansine类各有2款,PBD类1款。
4、抗体偶联药物医保谈判情况
近年来,医保目录调整逐步走向常态化,调整频率为一年一次。2022年9月6日,国家医保局发布《2022年国家医保药品目录调整通过初步形式审查药品及信息》,344个品种入围,涉及229家企业,符合调整条件的目录外品种共199个。
2022年的医保谈判中,共有4款抗体偶联药物(ADC)参与,包括1款目录内的荣昌生物维迪西妥单抗,以及3款目录外的跨国药企产品:罗氏恩美曲妥珠单抗、辉瑞奥加伊妥珠单抗和武田维布妥昔单抗。此外,吉利德戈沙妥珠单抗因获批上市时间晚于2022年6月30日无资格参与本次医保谈判。根据国家医保局和人力资源社会保障部于2023年1月18日印发的《2022年药品目录》,曲妥珠单抗、维布妥昔单抗和维迪西妥单抗被纳入目录,自2023年3月1日起正式执行。
行业竞争格局
1、区域竞争:长三角地区较为集中
根据区域热力图,我国抗体偶联药物行业产业链企业在长三角地区较为集中。其中,浙江代表有华东医药、
新码生物、浙江医药、多禧生物;江苏有恒瑞医药、东曜药业;上海有乐普生物、乐纯生物、奥浦迈等。
2、企业竞争:荣昌生物为国内首发出线
据统计,2021年除TIVIDAK、ZYNLONTA外的11种ADC药物合计销售额为52.5亿美元,2022年根据已公布10种药物的销售数据,合计营收约74.91亿美元,同比增长约42.69%。其中,销售额排名第一的药品是罗氏的Kadcyla,2021年销售额达21.31亿美元,2022年达22.88亿美元。其次是武田和Seagen研发的Adcetris,2022年营收达14.69亿美元。
我国本土企业荣昌生物研发的爱地希是我国目前唯一一个成功商业化的ADC药物,其2021年销售收入为0.13亿美元,截至2022年3月2日,荣昌生物业绩预告预计营收7.9亿元,营业利润亏损9.6亿元。除荣昌生物外,目前国内拥有ADC药物在研管线的药企还有恒瑞医药、石药集团、科伦药业、君实生物、浙江医药、复旦张江、乐普生物、豪森药业、百奥泰、东曜药业、多禧生物和上海美雅珂等。
注:1日元=0.00766美元;1瑞士法郎=1.1001美元;1英镑=1.21美元Tividak、Zynlonta
2021销售时间过短,暂不进行同比比较。
行业发展前景及趋势预测
1、抗体偶联药物发展趋势
根据科伦博泰招股说明书,凭藉ADC设计及偶联技术的不断进步,截至2022年底,全球共有15款ADC药物获监管部门批准上市,ADC已从晚期治疗特定血癌发展到有可能治疗更广泛实体瘤适应症及其他疾病的早期治疗方式。

2、抗体偶联药物行业市场规模预测
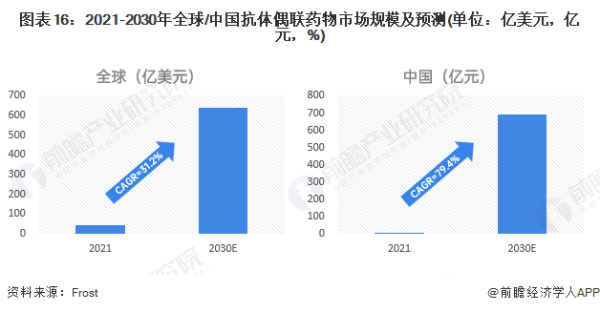
根据Frost&Sullivan,ADC的全球市场规模自2017年的16亿美元快速增长至2021年的55亿美元,年复合增长率为35.9%,并预计于2021年至2030年仍将以31.2%的增长率持续快速增长。在中国市场,自国家药监局批准首款ADC药物Kadcyla后,国内ADC药物市场于2020年开始增长,预期由2021年起以79.4%的年复合增长率增长,到2030年将达689亿元。
以上数据来源于前瞻产业研究院《中国抗体药物偶联物(ADC)行业市场前瞻与投资战略规划分析报告》。







